CLASE DEL 18 DE NOVIEMBRE DE 2015
Hola queridos estudiantes:
Actividades de nivelación: De 2:00 pm a 4:00 p.m
Favor llevar diligenciado y estudiado el taller de nivelación, que a continuación se relaciona.
Espero realices estas actividades con dedicación.
En clase:
Prepárate desde casa para la evaluación del átomo, entrando a los siguientes link e interactuando con las actividades allí propuestas.
Presenta estas actividades en el cuaderno. No olvides estudiar para la sustentación.
1° Compara los modelos atómicos de Daltón, Thomson, y rutherford y escribe cinco diferencias:
Modelo Atómico de Dalton
|
Modelo Atómico de Thomson
|
Modelo Atómico de Rutherford
|
2° Realiza la distribución electrónica con el respectivo dibujo a cada uno de los elementos que pertenecen a los grupos: IA, IIA, IIIA, IVA, VA, VIA y VIIA de la tabla periódica.
3° Define los siguientes términos:
Electrón
Protón
Neutrón
Número Atómico
Masa Atomica
Nivel
Subnivel
Orbital
Electrón
Protón
Neutrón
Número Atómico
Masa Atomica
Nivel
Subnivel
Orbital
4° Determine masa atómica, numero atómico, neutrones, electrones
Elemento
|
Z
|
A
|
N
|
E
|
Li
|
3
|
4
| ||
N
|
14
|
7
| ||
F
|
9
|
19
| ||
B
|
5
|
6
|
5° Elabora el cartel ecológico teniendo en cuenta las pautas dadas en clase.
Y AHORA SOLO FALTA ........................GRADUARSE....
CLASE DEL 11 DE NOVIEMBRE DE 2015
Hola queridos estudiantes:
A continuación relaciono las actividades a resolver:
En casa:
Nota:
Cuando el símbolo del elemento esta acompañado de una carga negativa, al número de e- se le aumenta lo correspondiente a la carga negativa:
Ej:
-2
16S:
p+: 16
e-: 18
no: 16
Cuando el símbolo del elemento esta acompañado de una carga positiva, al número de e- se le resta lo correspondiente a la carga positiva:
Ej:
+2
12Mg:
p+: 12
e-: 10
no: 12
Completar las siguientes tablas:
7.
Taller de
repaso Tema: “EL ATOMO”
1º
Diga si es Falso o verdadero, argumentando las afirmaciones falsas:
a. Los
protones se localizan en la periferia del átomo. ( )
_________________________________________________________________________________________________________________________________________________
b. Al
sumar protones con electrones se determina la masa del átomo ( )
__________________________________________________________________________________________________________________________________________________
23
c. Los
neutrones que presenta el átomo de
Na son 11 ( )
11
__________________________________________________________________________________________________________________________________________________
31
d. El
numero de protones que presenta el átomo de P
es 10 ( )
15
_________________________________________________________________________
_________________________________________________________________________
f. Los
àtomos presentan 5 niveles de energía representados con las letras: K, L, M, N,
O. (
)
__________________________________________________________________________________________________________________________________________________
2º Completa el siguiente mapa conceptual:
3º Completa la siguiente tabla:
Elemento
|
A
|
Z
|
no
|
P+
|
e-
|
80
Br
35
|
|||||
__
Cl
__
|
18
|
17
|
|||
___
K
__
|
39
|
19
|
|||
___
Fe
___
|
30
|
26
|
4º Realiza la
distribución electrónica a los elementos del punto anterior dibujando su
respectivo modelo atómico:
EN CLASE:
Evaluación del átomo.
Revisión y valoración de los átomos de los elementos asignados en clase.
Traer un pliego de cartulina, ega, plastilina y palillos pequeños. Lo puedes traer junto con otro estudiante o individual si lo prefieres.
NOTA:
Aun no se han recibido comentarios en el blog, respecto a problemática, personajes, mensaje y final de la película water wold. Espero sus comentarios.
Para los estudiantes que tienen actividades pendientes por entregar las recibiré sin falta para el 18-11-15, acompañada de una evaluación para nivelar los desempeños bajos.
CLASE DEL 04 DE NOVIEMBRE DE 2015
Hola queridos estudiantes:
A continuación relaciono las actividades a resolver:
En casa:
1° Completar la siguiente información:
2° Resolver en el cuaderno las siguientes preguntas, hazlo en lo posible sin ayuda de ningún texto ni Internet:
1.- ¿Cuáles son las partículas fundamentales del átomo?
2.- ¿Qué carga tienen esas partículas?
3.- ¿Qué masa tienen esas partículas?
4.- ¿Cuándo tenemos los cuerpos cargados?
5.- ¿Dónde se encuentran dentro del átomo cada una de esas
partículas?
6.- ¿Cómo se distribuyen los electrones dentro del átomo?
7.- ¿En qué se diferencian los átomos de los diferentes
elementos?
8.- ¿Qué es la masa atómica relativa media de un elemento?
9.- ¿Qué es un isotopo?
10.- Describe el modelo atómico de Bohr.
3° Resolver en el cuaderno los ejercicios propuestos en el siguiente link:
4° Proyecto transversal:
Ingresa al siguiente link y observa la película Water wold y participa en clase resolviendo las preguntas propuestas por la docente. Deja tu comentario en el blog ya que se valorará en la planilla de calificaciones.
EN CLASE:
1° Terminar el modelo atómico a los elementos dados en la clase anterior.
2° Resolver la siguiente actividad:
1.
1° Explique la diferencia entre los
isótopos de los siguientes elementos. Indica número atómico y número de
protones, número de electrones, número de neutrones y número másico.
a.
37 35
17Cl 17Cl
b.
12
13
6C 6C
c.
20 22
10Ne 10Ne
d.
54
57
26Fe 26Fe
e.
24
26
12Mg 12Mg
2. 2° Indique
cantidad de protones, neutrones y masa atómica en los siguientes Isóbaros
a.
40
40
20Ca 18Ar
b.
40
40
19K 20Ca
c.
14
14
6C 7N
d. 122
122
50Sn 52Te
e.
57 57
26Fe 27Co
3. 3° Indique
la masa atómica de cada uno de los elementos,
la cantidad de átomos presentes y
la masa molecular de los siguientes compuestos. (No olvide escribir el nombre
de cada uno de ellos).
a.
Al(OH)3
b.
CaCl2
c.
CaCO3
d.
CO2
e.
CuSO4
f.
Fe2O3
g.
H2O
h.
H2SO4
i.
KNO3
j.
NaCl
k.
NaHCO3
l.
NaOH
m.
NH3
n.
NO2
Quiz ingresando al siguiente link:
CLASE DEL 28 DE OCTUBRE DE 2015
Hola queridos estudiantes:
A continuación relaciono las actividades a resolver:
En casa:
1° Realiza en el cuaderno la distribución electrónica a los siguientes elementos, indicando electrones por niveles y el respectivo dibujo.
Ayúdate con la siguiente tabla
Cobalto
Vanadio
Silicio
Bromo
Galio
Arsénico
Magnesio
Rubidio
Estaño
Azufre
2° Define los siguientes términos:
Electrón
Protón
Neutrón
Número Atómico
Masa Atómica
Nivel
Subnivel
Orbital
3° Identifica los siguientes modelos atómicos y escribe su respectivo nombre sobre la línea:
_________________________________________________________________________________
_________________________________________________________________________________
_________________________________________________________________________________
4° Compara los modelos atómicos de Daltón, Thomson, rutherford y Bhor , escribe cinco diferencias:
5° Traer para la clase el siguiente material organizado en grupos de dos estudiantes:
Electrón
Protón
Neutrón
Número Atómico
Masa Atómica
Nivel
Subnivel
Orbital
3° Identifica los siguientes modelos atómicos y escribe su respectivo nombre sobre la línea:
_________________________________________________________________________________
_________________________________________________________________________________
_________________________________________________________________________________
4° Compara los modelos atómicos de Daltón, Thomson, rutherford y Bhor , escribe cinco diferencias:
Modelo Atómico de Dalton
|
Modelo Atómico de Thomson
|
Modelo Atómico de Rutherford
|
5° Traer para la clase el siguiente material organizado en grupos de dos estudiantes:
Lana
Lentejuela
1 pliego de cartulina
Ega o silicona líquida
3 bolas de icopor medianas partidas por la mitad
Plastilina de colores
En clase:
Prepárate desde casa para la evaluación del átomo,
entrando a los siguientes link e interactuando con las
actividades allí propuestas.
Elaborar los modelos atómicos empleando el material solicitado para la clase, a los elementos asignados por la docente en clase.
CLASE DEL 21 DE OCTUBRE DE 2015
Felicidades a María Camila Bastidas Ibagón y a María José Artega Urueña por el interés puesto en la realización y presentación de las actividades extraclase.
Felicidades a JUAN JOSE TOVAR LEIVA por sus conocimientos en Tabla Periódica.
Hola queridos estudiantes:
A continuación relaciono las actividades que desarrollarás en:
En Casa:
Registra en el cuaderno la siguiente información:
Registra con fotos los resultados de la experiencia. Imprímelo o envíalo al correo. Reúne el siguiente material:
2 tubos de PVC de 10 cm de largo
Pañuelos de papel
Dos globos
Un trozo de lana
PROCEDIMIENTO:
Deben atar el trozo de lana o hilo a uno de los tubos de PVC, luego frotar el tubo de PVC con el pañuelo seco durante treinta o cuarenta segundos.
Sujetar el tubo atado por la cuerda, hilo o lana y acercar el otro tubo. Observa, dibuja y explica lo que ocurre.
Inflar el globo y frotarlo con el pañuelo. Acercar otro globo. Observa, dibuja y explica lo que ocurre.
Ahora frota los dos globos. Observa, dibuja y explica lo que ocurre.
Lee atentamente la siguiente información y luego resuelve las preguntas que están a continuación:
Resuelve la siguiente actividad:
Observa las siguientes imágenes y luego resuelve las preguntas que están a continuación:
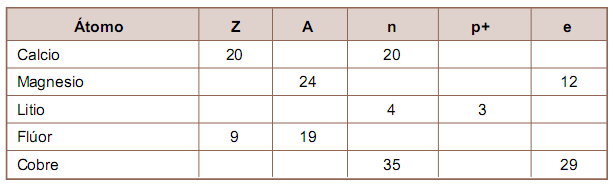
ÁTOMO DE CALCIO
ÁTOMO DE OXIGENO
ÁTOMO DE CLORO
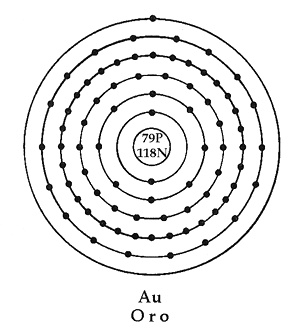
ÁTOMO DE ORO
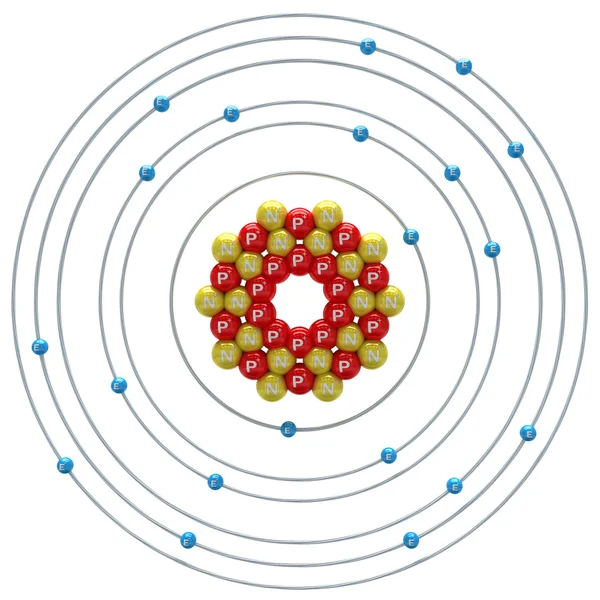
ÁTOMO DE FÓSFORO
Señala e identifica con flechas para cada elemento los protones, electrones y neutrones.
Completa la siguiente tabla:
Elemento
|
P+
|
e-
|
no
|
Cloro
| |||
Fósforo
| |||
Calcio
| |||
Oro
| |||
Oxígeno
|
Completa la siguiente información:
Átomo de Cloro:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Oxígeno:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Fósforo:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Calcio:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Oro:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Estudia para evaluación del tema "el átomo"
ACTIVIDADES PARA DESARROLLAR EN CLASE:
Registra en el cuaderno las siguientes actividades para ser resueltas en clase:
CLASE DEL 14 DE OCTUBRE DE 2015
En Casa:
Estudiar los primeros 30 elementos de la tabla periódica. Así:
Hidrógeno, Helio, Litio, Berilio, Boro, Carbono, Nitrógeno, Oxígeno, Flúor, Neón, Sodio, Magnesio,Aluminio, Silicio, Fósforo, Azufre, Cloro, Argón, Potasio, Calcio, Escandio, Titanio, Vanadio, Cromo, Manganeso, Hierro, Cobalto, Níquel, Cobre, Zinc.
En el colegio:
Resolveremos las actividades propuestas para la clase del 30-09-15.
Y NO OLVIDEN LOS COMPROMISOS PENDIENTES.........
Clase del 30-09-15
Hola mis apreciados estudiantes:
Hoy estudiaremos el átomo..........
ACTIVIDADES PARA RESOLVER EN CASA:
Organiza la exposición del modelo atómico asignado en clase. Expón con dominio y mucha naturalidad. Elabora diapositivas y trae el modelo hecho con mucha creatividad e imaginación.
Trae las evidencias (fotos o video) de las técnicas de separación de mezclas, junto con las respuestas a las preguntas del trabajo solicitado para hoy desde hace ocho días. Organizalo en una carpeta.
ACTIVIDADES PARA RESOLVER EN CLASE:
TALES DE MILETO
La carga eléctrica constituye una propiedad fundamental de
la materia. Se manifiesta a través de ciertas fuerzas, denominadas
electrostáticas, que son las responsables de los fenómenos eléctricos.
El término eléctrico, y todos sus derivados, tiene su origen
en las experiencias realizadas por Tales de Mileto.
Tales de Mileto fue un filósofo griego que vivió en el siglo sexto antes de Cristo. Tales estudió el comportamiento de una resina fósil, el ámbar (en griego elektron), observando que cuando era frotada con un paño de lana adquiría la propiedad de atraer hacia sí pequeños cuerpos ligeros, estos fenómenos se denominaron fenómenos eléctricos y más recientemente fenómenos electrostáticos.
Hagamos la experiencia:
Por parejas.
2 tubos de PVC de 10
cm de largo
Pañuelos de papel
Dos globos
Un trozo de lana
PROCEDIMIENTO:
Deben atar el trozo de lana o hilo a uno de los tubos de
PVC, luego frotar el tubo de PVC con el
pañuelo seco durante treinta o cuarenta segundos.
Sujetar el tubo atado por la cuerda, hilo o lana y acercar el
otro tubo. Observa, dibuja y explica lo que ocurre.
Inflar el globo y frotarlo con el pañuelo. Acercar otro
globo. Observa, dibuja y explica lo que
ocurre.
Ahora frota los dos globos. Observa, dibuja y explica lo que
ocurre.
Observa las siguientes imágenes y luego resuelve las preguntas que están a continuación:
ÁTOMO DE CALCIO
ÁTOMO DE OXIGENO
ÁTOMO DE CLORO
ÁTOMO DE ORO
ÁTOMO DE FÓSFORO
Señala e identifica con flechas para cada elemento los protones, electrones y neutrones.
Completa la siguiente tabla:
Elemento
|
P+
|
e-
|
no
|
Cloro
|
|||
Fósforo
|
|||
Calcio
|
|||
Oro
|
|||
Oxígeno
|
Completa la siguiente información:
Átomo de Cloro:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Oxígeno:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Fósforo:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Calcio:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Átomo de Oro:
Número de niveles:_____
Electrones por niveles:
Nivel K:_______
Nivel L:_______
Nivel M:_______
Nivel M:_______
Nivel N:_______
Clase del 23 de septiembre:
Hola mis queridos estudiantes:
A continuación relaciono las siguientes actividades:
Para resolver en CASA:
Ingresa al siguiente link
http://odas.educarchile.cl/objetos_digitales/odas_ciencias/22_jugando_separar/LearningObject/index.html y practica en casa las actividades allí sugeridas, ya que en clase se observará y evaluará.
Luego pon en practica lo aprendido, resolviendo la siguiente actividad:
Presentar en un informe escrito para el 30 -09 -15 y en grupos de dos estudiantes (si lo deseas) el desarrollo de la siguiente actividad:
Si deseas puedes ingresar al siguiente link en donde se encuentran las preguntas a continuación sugeridas.
Realiza y clasifica las siguientes mezclas:
A) Una mezcla con aserrín y sal.
1. ¿Qué tipo de mezcla es?
2. ¿Con que método separamos el serrín y la sal?
3. ¿Qué material podemos utilizar?
4. Haz un dibujo aplicando el método de separación. Pueden servir fotos.
B) Una mezcla de lentejas y clavos.
1. ¿Qué tipo de mezcla es?
2. ¿Con qué método podemos separar las lentejas y los y los clavos?
3. ¿Con qué material realizamos la separación de la
mezcla?
C) En esta experiencia necesitaras:
Una botella de plástico, un puñado de arroz,
lentejas, y garbanzos.
El procedimiento será el siguiente:
……………………………………………………………………………………………………………………...................................
en el recipiente de plástico y obtenemos una mezcla…………………………………………….
Propón tu otra mezcla de este tipo y elige
un método para separar sus componentes:
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
………………………………………………………………………………………………………
Una mezcla homogénea es aquella en la que no pueden
distinguirse los………………………………….
En esta 2ª experiencia necesitaras un vaso lleno de agua y una cucharada de azúcar.
El procedimiento será el siguiente:
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………
removemos y obtenemos una mezcla………………………………...
Propón tu otra mezcla de este tipo y elige
un método para separar sus componentes:
……………………………………………………………………………………………………………………
………………………………………………………………………
Expto. Separación de mezclas por imantación
1. Material que necesitaras:
limaduras de hierro, arena, un recipiente plano y un imán.
2. Procedimiento:
Mezclar la limadura de hiero con la arena en el recipiente.
Pasar el imán por encima de la mezcla.
3. Observación:
¿Qué pasa?.............................................
………………………………………………………………………………………………..
………………………………………………………………………………………………….
4. Explicación:
…………………………………………………………………………………………………
………………………………………………………………………
5. Dibujo o fotos de evidencia de la separación.
Expto. Separación de la sal y el agua
1. Material que necesitamos:
Sal, agua y un recipiente plano bastante grande.
2. Procedimiento:
Mezclamos el agua con la sal en el recipiente. Disolvemos bien hasta
que veamos que no admite mas sal.
Dejamos la mezcla al sol durante cuatro días.
3. Observación:
¿La mezcla que has preparado es homogénea o
heterogénea?..................................................................
¿Por qué?......................................................................
¿Qué pasa después de éste tiempo?
…………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………
4. Explicación:
……………………………………………………………………………………………………………………………………
5. Dibujo o foto de evidencia.
El tiempo necesario para completar el experimento depende:
a) de la temperatura ambiente
b) de la cantidad de agua
c) de la forma del recipiente de cristal.
Contesta:
La ……………………………….permite separar sustancias sólidas disueltas en el agua.
Una vez……………………….. el agua, en el fondo del recipiente queda la sustancia
disuelta.
La evaporación es mayor si …………………………….. la superficie del agua.
La evaporación es mayor si ………………………………. la cantidad de agua.
El tiempo que necesitamos para que se evapore toda el agua será
…………………….. si la temperatura ambiente es mayor.
Expto : separación de una mezcla de agua y azufre.
1. Material que necesitamos:
Azufre, agua, dos botellas de plástico, embudo y papel de filtro.
2. Procedimiento:
a) Mezclar el azufre con agua en una botella y agitamos
bien.
b) Colocar el embudo, con el papel de filtro encima, en
la segunda botella.
c) Finalmente vertimos sobre el filtro la mezcla de agua y
arena.
3. Observación:
¿Qué pasa?.............................................
………………………………………………………………………………………………..
………………………………………………………………………………………………….
4. Explicación:
…………………………………………………………………………………………………………………
………………………………………………………………………
5. Dibujo o fotos de evidencia
¿Qué otra mezcla se podría separar por filtración?
Tiza en polvo y agua………… sal y agua……………………
¿Cómo has sabido tu respuesta?..............................................................
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………….
Expto: separación de una mezcla de agua y glicerina
1.Material que necesitamos:
Agua, glicerina, dos botellas de plástico y un
vaso.
2. Procedimiento:
a) Mezclamos la glicerina y el agua en una botella y agitamos bien.
b) Dejamos reposar un tiempo la mezcla.
3. Observación:
¿Qué pasa?.............................................
………………………………………………………………………………………………..
………………………………………………………………………………………………….
Vuelve a girar la botella,¿qué pasa?........................
…………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………
4. Explicación:
…………………………………………………………………………………………………………………
………………………………………………………………………
La glicerina siempre quedará……………………ya que es menos denso que el agua.
Es exactamente lo mismo que ocurre cuando por accidente,
lamentablemente se derrama petróleo en los océanos ¿lo has notado?
Este mismo experimento lo puedes hacer con muchos otros
ingredientes. Por ejemplo, con un vaso con la mitad de agua y un poco de miel. Al tener la miel una densidad tan alta, se
mueve con mucha lentitud.¿Cuál es mas denso el agua o la miel?.............................................................
El aceite es menos denso que el vinagre. Por eso si los
mezclamos, la mezcla tiene dos capas, quedando el aceite en la parte………………..
Imagínate una pelota de plomo y otra exactamente igual de corcho. Si echáramos las dos pelotas en una piscina.¿Cuál de ellas flotaría?.................¿Por qué?.........................
……………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………..
Expto: El huevo que flota
1. Material que necesitamos:
Tres huevos frescos, agua, tres vasos de plástico
transparente, sal y una cuchara.
2. Procedimiento:
a) Echa unas ¾ partes de agua natural en cada uno de los vasos. Coloca los tres vasos con agua sobre una mesa.
b) En el primer vaso, añade 4 cucharadas grandes de sal y remueve durante unos 30 segundos con la cuchara.
c) Haz lo mismo con el segundo vaso y una vez listo, quita la mitad del agua salada y completa con agua natural.
d) Al tercer vaso no le añadas sal.
e) En cada uno de los vasos, añade 1 huevo y observa qué
sucede.
¿Qué sucede?
En el primer vaso (agua salada):…………………………………………….
En el segundo (½ agua salada y ½ agua natural)………………………
En el tercero (agua natural)………………………………………………………
4. Explicación:
¿Por qué ocurre esto?
Los huevos son más……………… que el agua dulce y se hunden en ella. Al disolver la sal en el agua aumentamos la ………………… de esta y por eso el huevo puede …………………….
¿Dónde es más fácil flotar en el mar o en la piscina?......... ¿Por qué?...........................................................
El Mar Muerto es uno de los más salados del mundo. A la gente le encanta ir allí,¿sabes por qué?.......................
……………………………………………………………………………………………………………….
Expto. Fabricamos estalactitas.
1. Material que necesitamos:
1 cacerola, 1 bote de sal fina, 1 cuchara sopera, 2 tarros de mermeladas vacíos, 1 cordel de nailon
trenzado de unos 30 cm de largo, 2 tuercas y 1 bandeja
2. Procedimiento:
a) Llenamos la cacerola con 1 litro de agua muy caliente.
b) Echamos 15 cucharadas soperas de sal.
c) Removemos hasta que la sal se disuelva.
d) Colocamos los tarros encima de la bandeja y llenamos con la disolución.
e) Ponemos una tuerca en cada extremo del cordel y lo
metemos en los tarros separando los tarros unos 15 cm
aproximadamente.
f) Presionamos sobre el cordel, entre los tarros, para crear un pequeño desnivel. Este permite que aparezca una gota y caiga cada 3 minutos, más o menos.
g) Las gotas no pueden aparecer ni demasiado rápido, ni
demasiado lento. Si las gotas aparecen muy despacio, acerca los tarros.
h) Colocamos la bandeja en lugar aislado durante una semana. Si queda poca agua en los tarros, rellena con más agua salada. Si es posible, es mejor realizar el experimento en un días calurosos ya que las altas temperaturas favorecen la evaporación.
Y a esperar.
3. Observación:
¿Qué pasa?.............................................
………………………………………………………………………………………………..
………………………………………………………………………………………………….
4. Explicación:
…………………………………………………………………………………………………
…………………………………………………………………………………………………
Dibuja o toma fotos.
Resolver en casa las siguientes preguntas de inducción al tema: planteadas en la clase pasada:
Cuando divides un terrón habrás observado que cada una de estas partículas se dividen a su vez, en partículas cada vez más pequeñas. Hasta dónde podría dividirse cada partícula sin que pierda sus propiedades? Explica
Cómo se llama la mínima unidad en la que puede dividirse la materia?
_______________________________________________________________________________________________________________________________________________________________________________________________________________
Haz escuchado hablar de la naturaleza eléctrica de la materia y la capacidad de algunos cuerpos de atraer a otros. Por ejemplo, cuando se frota un objeto y al acercarlo a trocitos de papel, estos son atraídos. ¿A qué se debe esto?
_______________________________________________________________________________________________________________________________________________________________________________________________________________
Toma un paquete de galletas y lee su etiqueta. Elabora una lista de los ingredientes usados para su fabricación.
_______________________________________________________________________________________________________________________________________________________________________________________________________________
¿La galleta corresponde a una sustancia pura o a una mezcla? Explica tu respuesta.
_______________________________________________________________________________________________________________________________________________________________________________________________________________Plantea tus hipótesis elaborando una lista de los componentes que conforman un refresco (gaseosa o jugo).
_______________________________________________________________________________________________________________________________________________________________________________________________________________
¿Los componentes del refresco se diferencian a simple vista? Qué tipo de mezcla es? Explica tu respuesta.
______________________________________________________________________________________________________________________________________________________________________________________________________________
En clase, daremos inicio al tema del átomo, observando el siguiente vídeo:
Con lo observado en los vídeos, completar la información solicitada en la siguiente tabla:
AUTOR
|
TEORIA PROPUESTA
|
Clase del 16-09-15
Hola mis pequeños gigantes de la ciencia:
En la clase de hoy desarrollaremos las actividades pendientes de la semana pasada:
1°Resolver la actividad del link
2°Evaluar los conocimientos adquiridos en el tercer período
3°Diligenciar la dimensión formativa.
4°Entrega de las competencias del cuarto período
5° Resolver en clase las siguiente preguntas de inducción al tema:
Cuando divides un terrón habrás
observado que cada una de estas partículas se dividen a su vez, en
partículas cada vez más pequeñas. Hasta dónde podría dividirse cada partícula
sin que pierda sus propiedades? Explica
Cómo se llama la mínima unidad en la que puede dividirse la materia?
_______________________________________________________________________________________________________________________________________________________________________________________________________________
Haz escuchado hablar de la
naturaleza eléctrica de la materia y la capacidad de algunos cuerpos de atraer a otros. Por ejemplo, cuando se frota un objeto y al
acercarlo a trocitos de papel, estos son atraídos. ¿A qué se debe esto?
_______________________________________________________________________________________________________________________________________________________________________________________________________________
Toma un paquete de galletas y
lee su etiqueta. Elabora una lista de los ingredientes usados para su
fabricación.
_______________________________________________________________________________________________________________________________________________________________________________________________________________
¿La galleta corresponde a una
sustancia pura o a una mezcla? Explica tu respuesta.
_______________________________________________________________________________________________________________________________________________________________________________________________________________Plantea tus hipótesis
elaborando una lista de los componentes que conforman un refresco (gaseosa o
jugo).
_______________________________________________________________________________________________________________________________________________________________________________________________________________
¿Los componentes del refresco
se diferencian a simple vista? Qué tipo de mezcla es? Explica tu respuesta.
______________________________________________________________________________________________________________________________________________________________________________________________________________
Clase del 09-09-15
Hola experimentores
En vista de que no nos vimos esta semana y como el período finaliza el 11-09, la clase de hoy se desarrollará lo programado para la clase del 02-09, ademas se realizará evaluación final de período, por ello les recomiendo repasar los temas vistos en el período y revisar de nuevo el blog.
Los cuadernos se enviarán el próximo 04-09.
Favor imprimir el siguiente documento para trabajarlo en
grupos de 2 estudiantes en la clase:
Copiar en el cuaderno o imprimir el siguiente formato y
diligenciar la autoevaluación y coevaluación.
CRITERIO
|
AUTO
EVALUACION
|
COE
VALUACION
|
HETERO
EVALUACION
| |
1
|
Busco la excelencia en el desarrollo ypresentación de tareas y trabajos.
| |||
2
|
Asisto puntualmente a clase y recibo a la docente en mi respectivo puesto.
| |||
3
|
Presento buena disposición en clase, soy atento y participativo.
| |||
4
|
Me preparo con anterioridad en las evaluaciones programadas.
| |||
5
|
Mantengo buena disciplinadurante todala clase.
| |||
6
|
Respeto a compañeros ydocente.
| |||
7
|
Soy solidario con mis compañeros.
| |||
8
|
Acato las normas de presentación personal establecidas por la Institución.
| |||
9
|
Soy ordenado y aseado con mi entorno.
| |||
10
|
Cumplo oportunamente con las actividades extra clase.
| |||
TOTAL
|
Acciones de Mejora:
Acciones Correctivas:
Acciones Preventiva:
Clase del 02-09-15
Las actividades que quedaron pendientes por desarrollar en la clase del 26-08-15 las trabajaremos en la clase de hoy. En clase les entrego los cuadernos.
Favor llevar los materiales solicitados en la guía junto con: Aceite, glicerina, sal, alcohol, azufre, bicarbonato de sodio, azúcar.
GUÍA DE LABORATORIO: MÉTODOS DE SEPARACIÓN DE MEZCLAS
TEMA: Métodos de separación de mezclas
Objetivo:
Aplicar técnicas para separar mezclas homogéneas y heterogéneas a sustancias del entorno, mediante el reconocimiento de las propiedades de sus componentes a separar.
Separación de mezclas homogéneas Evaporación:
Materiales e implementos
Bata, Cloruro de sodio, agua, tubos de ensayo, mechero de alcohol, agitador, pinzas de madera.
Procedimiento:
Toma un tubo de ensayo y agrega 3 ml de agua, luego 10 g de cloruro de sodio, mezcla con el agitador hasta obtener una mezcla homogénea. Toma el mechero, enciende y acerca el tubo de ensayo presionado con la pinza, hasta que el cloruro de sodio precipite, cuando el agua haya evaporado.
Separación de mezclas heterogéneas. Imantación:
Materiales e implementos.
Imán, harina de trigo, limadura de hierro, caja de petri, espátula.
Procedimiento:
Toma la caja de petri, coloca un poco de harina de trigo, luego agrega limaduras de hierro, mezcla y acerca el imán hasta separarse el hierro.
Filtración
Materiales e implementos:
Papel filtro, embudo, beaker, agua, arena , agitador.
Procedimiento:
Realiza una mezcla de agua y bicarbonato de sodio, prepara el embudo con el papel filtro siguiendo las instrucciones del docente, luego vierte la mezcla y recoge el liquido en el beaker.
Decantación de sólidos:
Materiales e implementos:
Papel filtro, embudo, beaker, agua, arena , agitador.
Procedimiento:
Realiza una mezcla de agua y arena, agita y deja sedimentar el precipitado,
luego vierte la mezcla y recoge el liquido en otro beaker.
Decantación de líquidos:
Materiales e implementos.
Embudo de decantación, aceite, agua, beaker.
Procedimiento:
En el embudo de decantación agrega 150 ml de agua, agrega 50 ml de aceite, manipula la llave y deja decantar el agua, cuando esta haya salido completamente cierra la llave.
Tamizado:
Materiales e implementos:
Tamiz (coladera), arena, piedras pequeñas, valde.
Procedimiento.
Toma la arena y mezcla con la piedra pequeña. Hasta pasarla por el tamiz o coladera hasta quedar solamente piedras en el tamiz.
Resuelve:
1. Describe el procedimiento utilizado en cada experiencia y los materiales e implementos. Para ello sigue el orden de la guía-
2. Que características se destacan en cada sustancia que les permita separarse por métodos físicos.
3. Establece diferencias entre métodos físicos y químicos.
4. Representa mediante dibujos cada montaje realizado en la experiencia.
5. Dibuja los implementos utilizados en la experiencia-
Definir: Sustancias miscibles, sustancias in miscibles, solubilidad, fases, homogéneo y heterogéneo
Completar la siguiente información:
Sustancia A
|
Sustancia B
|
Tipo de Mezcla
|
Técnica de separación
|
Montaje
|
No olvides llevar la bata y los demás materiales de seguridad solicitados para las prácticas de laboratorio. Para tu aseo personal leva jabón y una toallita.
CLASE DEL 26-08-15
Aprovecho para felicitarlos con un abrazo de oso giganteeeeeeeeee por el excelente compromiso mostrado en las olimpiadas del SABER.
Niños(as) las actividades programadas para el 19-08 se realizarán en la clase del 26-08-15
Clase del 19-08-15
Niños y Niñas del grado QUINTO, los quiero felicitar por la buena disposición y ganas de aprender. Los quiero mucho.....
Actividades a desarrollar en clase:
1° Socializar el taller publicado el 05-08
2° Resolver el ejercicio 3 de la actividad propuesta a realizar en casa publicado el 05-08
3° Observar el siguiente vídeo.
4° Con lo que aprendiste del vídeo, completa la información solicitada en la siguiente tabla:
Mezcla
|
Estado de los componentes
|
Solubilidad
|
Tipo de mezcla
|
técnica de separación
|
Montaje
|
1
|
|||||
2
|
|||||
3
|
|||||
4
|
|||||
5
|
|||||
6
|
|||||
7
|
|||||
8
|
|||||
9
|
|||||
10
|
Explica la siguiente afirmación:
Por qué es necesario conocer el estado físico, características y propiedades de los componentes de una mezcla?
5° Práctica de laboratorio: Traer los siguientes materiales, recuerda que los puedes traer en grupo.
Imán
Colador (que ya no uses)
Toallita o bayetilla
2 hojas de papel filtro
Mechero de alcohol (si lo tienes)
Alcohol
Sustancia
A
|
Sustancia
B
|
Tipo de
Mezcla
|
Técnica
de separación
|
Montaje
|
No olvides llevar la bata y los demás materiales de seguridad solicitados para las prácticas de laboratorio. Para tu aseo personal leva jabón y una toallita.
NO HAY ACTIVIDADES PARA DESARROLLAR EN CASA, sin embargo repasa las experiencias vistas en clase, ya que muy pronto se evaluarán estos temas.
Clase del 12-08-15
En clase socializaremos las respuestas del taller resuelto en casa la semana pasada, ya que se aplicará quiz de los temas y prácticas de laboratorio realizadas este período, así que no olvides repasar un poco los apuntes.
Además se desarrollará en clase el taller que quedo pendiente por resolver en la clase pasada.
Organizados en grupos de dos estudiantes consigue los siguientes materiales para realizar una interesante práctica de laboratorio:
Aceite de cocina
Glicerina
Miel
Vinagre
Alcohol
Sal
Azucar
Bicarbonato de sodio
Azufre
Limadura de hierro
Leche
Jugo de limon
Llevar copiado o impreso en el cuaderno de laboratorio la siguiente tabla:
Sustancia A
|
Sustancia B
|
Estado
Sustancia A
|
Estado
Sustancia B
|
Propiedades Físicas
Sustancia A
|
Propiedades
Físicas Sustancia B
|
No. De fases
|
Tipo de Mezcla
|
Clase del 05-08-15
ACTIVIDAD PARA RESOLVER EN CASA:
Resolver en el cuaderno
1. Con una X sobre la letra marque
la respuesta correcta una y solo una respuesta:
1. Los
Procesos físicos, actúan sobre la materia:
a. Transformándola b. Cambiando
sus propiedades físicas.
c. No
le cambian sus propiedades
físicas. d. Ninguna
de las anteriores.
2. La
masa es:
a. Cantidad
de materia
b. La
densidad de la materia
c. El
peso de la
materia d. Ninguna
de las anteriores.
3. Son
estados fundamentales de la materia:
a. Sólido
y
líquido b. Gaseoso
y coloidal
c. Sólido,
líquido, gaseoso y
plasma
d. Plasma
y coloidal
4. Los
coloides son:
a. Estados
fundamentales de la
materia b. Estados
intermedios de la materia
c. Estado
vesicular de la
materia d.
Ninguno de los anteriores.
5. En
el estado sólido las fuerzas de las moléculas son:
a. De atracción menor que de
repulsión b. De
atracción igual que de repulsión
c. De repulsión mayor que de
atracción d.
Las fuerzas de las moléculas no existen
6. Sustancias
formadas por la misma clase de átomos de denominan:
a. Moléculas b. Elementos
químicos
c. Compuestos
químicos d. Gases
7. Ductilidad
es la propiedad que presentan los cuerpos para:
a. Dejarse convertir en
láminas b. Combinarse
fácilmente con otro cuerpo
c. Poderse separar por medios
mecánicos d. Dejarse convertir
en hilos.
8. El agua es:
a. Un elemento químico
b. Un compuesto químico
c. Una solución
d. Una mezcla
9. El aire es:
a. Un elemento químico
b. Un compuesto químico
b. Una mezcla homogénea
c. Una mezcla heterogénea
10. La temperatura se mide con:
a. El termómetro
b. La balanza
c. El dinamómetro
d. El barómetro.
11. Una sopa de legumbres es:
a. Un elemento químico
b. Un compuesto química
b. Una mezcla homogénea
c. Una mezcla heterogénea
12. El cambio de estado de gas a
líquido se denomina:
a. Condensación b.
Fusión
c. Sublimación d. Condensación
2. A. Identifique como
propiedad física (F) o como propiedad química (Q) lo siguiente:
1. _____ Una botella de gaseosa se empaña
al retirarla de la nevera
2. _____ La gasolina de enciende en los
cilindros de un motor
3. _____ Un clavo de hierro es atraído por
un imán
4. _____ Un helado se derrite cuando se
expone al sol
5. _____ El éter es una sustancia
fácilmente inflamable
6. _____ El agua es incolora
7. _____ Al quemar el papel se transforma
en carbón
8. _____ Juanita tiene los ojos
verdes
9. _____ El alcohol es un líquido de olor
fuerte
10. _____ Los metales en presencia del
oxígeno se oxidan
2.B. Clasifique
los siguientes cambios como físicos (F) o como químicos (Q)
1. _____ Formación de nubes en la
atmósfera
2. _____ Putrefacción de la carne
3. _____ Fusión del hielo de los casquetes
polares
4. _____ Proceso de la digestión
5. _____ Combustión de la madera
6. _____ Preparar café con leche
7. _____ La carne se volvió carbón
8. _____ Solidificación del agua
9. _____ Ruptura de vasos sanguíneos
10. _____ Incendio forestal
3A. Completa la siguiente tabla con una
X en el cuadro correspondiente
Sustancia
|
Mezcla
|
Sustancia pura
|
||
Heterogénea
|
Homogénea
|
Compuesto
|
Elemento
|
|
Azúcar
|
||||
Agua de
mar
|
||||
Aire
|
||||
Mayonesa
|
||||
Gasolina
|
||||
Hielo
seco
|
||||
Amoniaco
|
||||
Detergente
|
||||
Alambre
de cobre
|
||||
Gas que
expele el exhosto de un auto
|
||||
4. A. Escriba
como se llama los siguientes cambios y si se requiere aumento o disminución de
temperatura:
a. Sólido a líquido:
___________________________La temperatura _____________________
b. Líquido a gas:
___________________________La temperatura _____________________
c. Gas a
sólido:
___________________________La temperatura _____________________
d. Líquido a
sólido: ___________________________La temperatura
_____________________
e. Gas a líquido: ___________________________La
temperatura _____________________
Completa la siguiente tabla:
Aspecto
|
Estado
sólido
|
Estado
líquido
|
Estado
gaseoso
|
Ordenamiento
de las partículas
|
|||
Movimiento
|
|||
Cercanía
de las partículas
|
|||
Fuerzas
intermoleculares
|
|||
Volúmen
y forma
|
ACTIVIDAD PARA RESOLVER EN CLASE
1° Preparar las siguientes mezclas:
Yogur de mora:
Grupo de:
Camila: 3 bon yurt, 10 vasos plásticos desechables
Laura: Mora melada picada, un recipiente para mezclar.
María José: 1 botella de leche de vaca hervida (Tibia)
Limonada:
Andrés Felipe: 1 bolsa de limones
Jaime Alberto: 1 libra de azúcar
Brayan: 1 bolsa de hielo
Juan José: Recipiente para mezclar, 1 cucharon y 10 vasos desechables
2° Traer:
Bolsita de azufre
Parafina
Tapitas metálicas sin plástico
No olvides llevar los implementos de seguridad para las prácticas de laboratorio.
3° Observar el siguiente vídeo:
3° Clasificar:
Traer anotado en el cuaderno:
Traer anotado en el cuaderno:
Sustancia
|
Propiedad
|
P. Física
|
P.
Química
|
|||
Extensiva
|
Intensiva
|
organolépticas
|
General
|
Especifica
|
||
El agua
es incolora
|
||||||
El agua
ebulle a 100°C
|
||||||
Los
metales se oxidan con facilidad.
|
||||||
500 g
de Sulfato férrico
|
||||||
1L de
Ácido Sulfúrico
|
||||||
El
Hidróxido de Sodio reacciona con facilidad con el Ácido Clorhídrico para
formar Cloruro de Sodio (sal
|
||||||
El
ácido clorhídrico tiene sabor amargo
|
||||||
La
densidad del alcohol etílico (C2H5OH) es de 0.78 g/cc
|
||||||
Los no
metales reaccionan lentamente
|
||||||
El diamante ocupa el
puesto No. 10 en la escala de dureza de Mohs
|
||||||
El punto de fusión del
hierro es 1.538 °C
|
||||||
El cobre es dúctil
|
||||||
Los metales se oxidan facilmente
|
||||||
2. Establece claras diferencias entre:
Propiedad Física y Propiedad Químca
Propiedad General y Especifica
3. De las siguientes propiedades, cuáles son
generales y cuáles son especificas?
Incomprensibilidad de los solidos _______
Peso_____ Dureza_______ Brillo_____
Masa______ Porosidad________ Tenacidad_______
Color________ Volumen______
4. Cuáles son propiedades extensivas (son
propiedades que dependen de la cantidad de sustancia que se tome) o intensivas
(Son propiedades que no dependen de la cantidad de sustancia que se tome):
Volumen:________ Color:_________
Viscosidad:________ Densidad:_______
Masa:_______ Conductividad eléctrica:__________
Punto de fusión:_______
Inercia:_______ Brillo:________
Elasticidad:________ Dureza:_____________
5. Diferencie cuáles son compuestos y cuáles son
elementos:
H2O:______ H:_______ O3:_________ KMnO4:_____________ NH3:____________ CO:________
Hg:________
N2:_________ Cl:__________ Ca3(PO4)2:_____________Li:_____________
5.
Clasifique los siguientes cambios en Físicos o Químicos:
Oxidación
de una moneda:____________Hervir el agua:_______ Fotosíntesis:______ Fundir un
metal:_______ preparar una limonada:________ Formación de los óxidos en los
metales:_____________ Preparación de Kumis:________ Encender un
fósforo:___________ Derretir una paleta:___________ Congelar el
agua:______________
Clase del 29-07-15
Hola mis queridos estudiantes.
El PC de mi portátil sufrió serios daños..... pero tranquilos que ya se solucionó el problema. así que manos a la obra.
En la clase de hoy seguiremos experimentando con la materia, para ello consigue en pequeñas cantidades y en grupos de 3 estudiantes los siguientes materiales: Puedes hallarlos con facilidad en una chatarrería.
Cobre, aluminio, hierro (en limaduras), azufre, carbono, plata, zinc y plomo.
Con estos materiales vamos a estudiar sus propiedades tanto físicas como químicas. Las observaciones se registrarán en la siguiente tabla (por favor traerla anotada en el cuaderno de laboratorio).
Propiedades físicas:
Elemento
|
Símbolo
|
Color
|
Olor
|
Textura
|
aspecto
|
Brillo
|
Dureza
|
Fragilidad
|
Tenacidad
|
Densidad
|
P. Fusión
|
P. ebullición
|
Propiedades Químicas:
Sustancia
|
Ácido Clorhídrico
|
Ácido Acético
|
Cambios de la materia:
10 tapas de gaseosa sin plástico
1 cucharadita de azufre
Alcohol
Parafina de una vela
Sal
Azúcar
Leche
Jugo de limón
Sustancia
|
Observaciones iniciales
|
Observaciones finales
|
Tipo de cambio
|
HOLA MIS EXPERIMENTORES. MIL DISCULPAS. CREO QUE ME ATACO EL VIRUS DEL ZICA. MI CUERPO NO SE SENTÍA PARA NADA BIEN. MUCHACHOS PROTEJANSEN LO NECESARIO, POR QUE ESTA ENFERMEDAD GENERA MUCHO DOLOR Y MALESTAR.
LO PROGRAMADO PARA EL 15-07, LO DESARROLLAREMOS EN LA CLASE DE LA PRÓXIMA SEMANA. RECIBO FRUTAS.......JAJAJA
CLASE DEL 15 -07-15
Hola mis experimentores.
Los espero en clase con los materiales solicitados para la clase del 8-07-15.
En clase realizaremos las prácticas propuestas que permitan comprender con facilidad y agrado las propiedades de la materia.
De igual manera se experimentará con la temperatura. Para ello se les solicita llevar los siguientes materiales:
1 bolsa de leche
1 bolsa de crema de leche
1/2 libra de azúcar
Fresa melada
Por favor llevar apuntado en el cuaderno la siguiente guía de laboratorio.
Pregunta problematizadora
|
Formulación de hipótesis
|
Observaciones
|
Resultados y/o conclusiones
|
CLASE DEL 8-07-15
En clase vamos a resolver las siguientes peguntas, apoyadas en sencillas y divertidas experiencias:
¿Cuáles son las propiedades generales y especificas de la materia?
Globos de diferentes formas y tamaños
Recipientes plásticos de diferentes formas y tamaños
¿Por qué flotan los barcos?
Materiales solicitados:
2 Láminas de papel aluminio
30 monedas
1 libra de sal
3 vasos plásticos trasparentes
1 huevo crudo
¿Por qué flota el hielo en el agua?
Materiales solicitados:
1 bolsa de hielo en cubos
4 cubos de hielo de colores
1 botella de alcohol
1 botella de soda
¿Por qué flota un sobre de mayonesa en el agua?
Materiales solicitados:
1 sobre personal de mayonesa
4 clips
1 botella plástica trasparente con una capacidad de 1 litro
Cinta plástica
¿Qué contiene una gaseosa?
Materiales solicitados:
1 lata pequeña de gaseosa
1 lata pequeña de gaseosa dietética
Qué es la densidad?
Materiales solicitados:
1/4 litro Aceite de cocina
1/4 litro de miel
1/4 litro de alcohol
1 bolsa pequeña de algodón
NOTA:
Los materiales solicitados los pueden traer en grupos de 3 estudiantes o individual.
Solo lleven a clase los materiales que más se les facilite.
HOLA DE NUEVO
Los espero en clase cargados de mucha energia, entusiasmo y la alegria de aprender cosas nuevas.
Actividades a realizar
en clase:
1° Copiar en el
cuaderno o imprimir el siguiente formato, para diligenciarlo en clase,
atendiendo las pautas de la educadora:
CRITERIO
|
AUTO
EVALUACION
|
COE
VALUACION
|
HETERO
EVALUACION
|
|
1
|
Busco
la excelencia en el desarrollo y presentación
de tareas y trabajos.
|
|||
2
|
Asisto puntualmente a clase y recibo a la docente en mi respectivo puesto.
|
|||
3
|
Presento buena disposición en
clase, soy atento y participativo.
|
|||
4
|
Me preparo con anterioridad en las
evaluaciones programadas.
|
|||
5
|
Mantengo buena disciplina durante toda la
clase.
|
|||
6
|
Respeto a compañeros y docente.
|
|||
7
|
Soy solidario con mis compañeros.
|
|||
8
|
Acato las normas de presentación
personal establecidas por la Institución.
|
|||
9
|
Soy ordenado y aseado con mi
entorno.
|
|||
10
|
Cumplo oportunamente con las
actividades extra clase.
|
|||
TOTAL
|
Acciones de Mejora:
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Acciones Correctivas:
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
2° Realizar las
siguientes mediciones:
Longitud:
Objeto
|
Regla: cm
|
Metro: m
|
Cuartas
|
Pasos
|
Lapicero
|
||||
Largo de la cancha
|
||||
Ancho de la cancha
|
||||
Estatura de un compañero
|
||||
Un dedo
|
||||
Un pie
|
||||
Laso
|
||||
Un árbol
|
||||
Cuarta
|
||||
Pasos
|
Tiempo: Cronometro (Favor llevar el cronometro a clase)
Segundos empleados al
caminar una distancia de 5 metros
Segundos empleados en
dar 5 vueltas a la cancha
Carrera de carretillas
Temperatura: (Favor
llevar un termómetro)
Medir la temperatura:
Del agua de la
alberca:_____________
Corporal
tuya:_____________
Corporal de un
compañero:___________
Del agua de la
llave:___________
.jpg)







































profe en esta clase vamos a hacer el helado? :D
ResponderEliminaro cuando?
ResponderEliminarespero que se recupere
ResponderEliminarprofeeeeeee. lo hago en el de quimica o laboratorio
ResponderEliminarprofeeeeeee. lo hago en el de quimica o laboratorio
ResponderEliminarprofe ddiga el nombre de el que gano al puebra saber
ResponderEliminarEl grupo de la niña Camila Bastidas
ResponderEliminarprofe hoy 9 de septiembre no puedo venir por que estoy en Ibague comprando la ropa de mi primera cumunion
ResponderEliminarLástima. Entonces lo de la clase lo evaluo en la proxima semana
ResponderEliminarprofe yo que de exonerado de la evaluación tengo 11 caras
ResponderEliminarCLARO
ResponderEliminarprofe la tarea que nos dejo en que cuaderno hay que escribirlo
ResponderEliminaren cual el de quimica? o el otro
ResponderEliminarEn el cuaderno de química
ResponderEliminarhola profe no puedo traer la tarea completa por que se me fue la luz y asta hora medi cuenta
ResponderEliminarhola profe no puedo traer la tarea completa por que se me fue la luz y asta hora medi cuenta
ResponderEliminarEste comentario ha sido eliminado por el autor.
ResponderEliminarProfe gracias por sus enseñanzas,aprendi mucho.Que Dios la bendiga.
ResponderEliminarGracias por el comentario. Espero verte el próximo año. Besos
Eliminarprofe jaime no hiso el quiz virtual tampoco hiso la tabla periódica ni las exposiciones y tampoco hiso la ultima tarea pendiente de los materiales ni el comentario del vídeo mejor dicho nada hiso este periodo........
ResponderEliminarLastima que no valoren el aprendizaje que se logra con la realización de actividades extraclase.
Eliminarprofe mire los espacios de el
ResponderEliminares verdad en no hiso nada l atarea de la clase pasada no la hiso ni la antepasada ni a anteantepasada ni la esposicion o lo de la tabla periodica no lo hiso jaime se esta poniendo muy fresco en su clase profe tiene que parar esto por que luego no hace ninguna tarea
ResponderEliminarperdonen la ortografia
ResponderEliminarLLOOOLOLOLLO
ResponderEliminar